ETS – De l’innovation au patient
Qu’est-ce que l’ETS?
L’évaluation des technologies de la santé (ETS) est un examen minutieux des technologies et des interventions en matière de santé afin de déterminer comment elles affectent notre santé, y compris leurs conséquences directes et indirectes [1]. L’objectif de ce processus multidisciplinaire est d’évaluer l’importance d’une technologie de santé et la manière dont elle peut être utilisée dans les systèmes de santé du monde entier [1]. Ce processus implique de nombreux experts issus de différents domaines, également connu sous le nom de processus multidisciplinaire. Ils utilisent des données probantes, dans le cadre d’un processus transparent et responsable, pour aider les décideurs, tels que les décideurs politiques, à faire des choix concernant les nouvelles technologies de la santé. Au Canada, l’Agence canadienne des médicaments et des technologies de la santé (ACMTS) est l’un des principaux organismes à but non lucratif chargés d’aider les décideurs en matière de santé à formuler des recommandations sur diverses technologies de la santé, telles que les médicaments, les tests de diagnostic et les procédures et dispositifs médicaux [2]. Elle formule des recommandations pour l’ensemble du Canada, à l’exception du Québec, où une autre agence, l’Institut national d’excellence en santé et en services sociaux (INESSS), est chargée de formuler des recommandations sur les technologies de la santé.
Pourquoi l’ETS est-elle importante pour les médicaments et les traitements innovants en oncologie ?
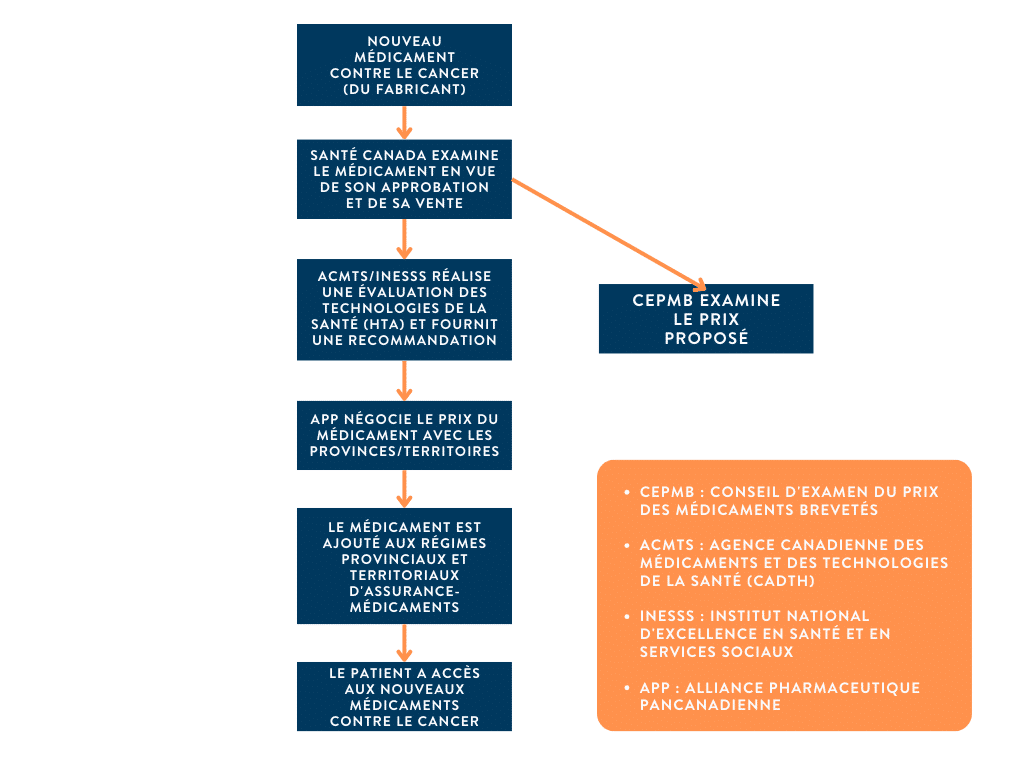
Les évaluations des technologies de la santé sont importantes pour les traitements oncologiques, car elles permettent aux patients d’avoir accès à de nouveaux traitements. Au Canada, par exemple, l’ACMTS et l’INESSS émettent des recommandations à savoir si les régimes de remboursement publics provinciaux et territoriaux devraient rembourser les nouveaux médicaments anticancéreux sur la base de la « valeur » qu’ils apportent à la santé publique [3]. Après avoir été approuvés par l’ACMTS et/ou l’INESSS, les médicaments sont soumis à l’Alliance pharmaceutique pancanadienne (APP) dans le but de négocier le prix des médicaments dans le cadre d’un régime public [3]. Si les négociations de prix entre l’APP et les fabricants de médicaments sont fructueuses, chaque province et territoire décidera alors d’ajouter ou non ces médicaments à son régime public de remboursement [3].
Il est important de savoir qu’avant que ces processus d’ETS puissent commencer, les fabricants de médicaments doivent soumettre leur produit à Santé Canada pour qu’il soit approuvé à la vente [3]. Suite à cette approbation, les fabricants de médicaments peuvent demander au Conseil d’examen du prix des médicaments brevetés (CEPMB), une agence fédérale, de réviser le prix suggéré. L’ensemble du processus d’ETS vise à assurer que des traitements efficaces sont disponibles et abordables pour les personnes atteintes d’un cancer, tout en tenant compte des coûts sociétaux de chaque traitement approuvé.
Pourquoi l’ETS est-elle importante pour les médicaments et les traitements innovants en oncologie ?
Les évaluations des technologies de la santé sont importantes pour les traitements oncologiques, car elles permettent aux patients d’avoir accès à de nouveaux traitements. Au Canada, par exemple, l’ACMTS et l’INESSS émettent des recommandations à savoir si les régimes de remboursement publics provinciaux et territoriaux devraient rembourser les nouveaux médicaments anticancéreux sur la base de la « valeur » qu’ils apportent à la santé publique [3]. Après avoir été approuvés par l’ACMTS et/ou l’INESSS, les médicaments sont soumis à l’Alliance pharmaceutique pancanadienne (APP) dans le but de négocier le prix des médicaments dans le cadre d’un régime public [3]. Si les négociations de prix entre l’APP et les fabricants de médicaments sont fructueuses, chaque province et territoire décidera alors d’ajouter ou non ces médicaments à son régime public de remboursement [3].
Il est important de savoir qu’avant que ces processus d’ETS puissent commencer, les fabricants de médicaments doivent soumettre leur produit à Santé Canada pour qu’il soit approuvé à la vente [3]. Suite à cette approbation, les fabricants de médicaments peuvent demander au Conseil d’examen du prix des médicaments brevetés (CEPMB), une agence fédérale, de réviser le prix suggéré. L’ensemble du processus d’ETS vise à assurer que des traitements efficaces sont disponibles et abordables pour les personnes atteintes d’un cancer, tout en tenant compte des coûts sociétaux de chaque traitement approuvé.
Figure 1. Aperçu des étapes de l’examen et du remboursement des nouveaux médicaments oncologiques
Situation actuelle de l’ETS au Canada
- Détient l’un des processus d’ETS les plus lents : 19e sur 20 pays de l’OCDE
- Le processus d’ETS du Canada est presque deux fois plus long que celui des pays comparables.
- Il faut en moyenne 732 jours pour avoir accès à des médicaments dans le cadre du régime public provincial/territorial, contre 226 jours pour avoir accès à ce même type de médicaments dans le cadre d’un régime privé (remboursé par l’assurance).
- Seul un nouveau médicament sur cinq, disponible à l’échelle mondiale, est remboursé par les régimes publics au Canada.
Qu’est-ce que les Marathons de remue-méninges (Hackathons) sur le traitement du cancer au Canada ?
Pour faire face aux défis associés à l’accès aux nouveaux traitements contre le cancer, Cancer colorectal Canada a lancé les « Marathons de remue-méninges sur le traitement du cancer au Canada ». Au cours de ces rencontres, des personnes clés impliquées dans l’ETS ont été invitées à examiner le processus actuel d’examen et de remboursement des traitements et à faire des suggestions novatrices pour accélérer l’accès des Canadiens à de nouveaux traitements novateurs.
Qui sont les participants aux Marathons de remue-méninges (Hackathons) de CCC (parties prenantes) ?
- Les groupes de patients
- Les responsables de l’évaluation des technologies de la santé
- Experts en politiques
- Leaders de l’industrie et experts économiques
- Des représentants du gouvernement
- Des chercheurs
- Des cliniciens.
Quel a été l’impact des précédents Marathons de remue-méninges (Hackathons) ?
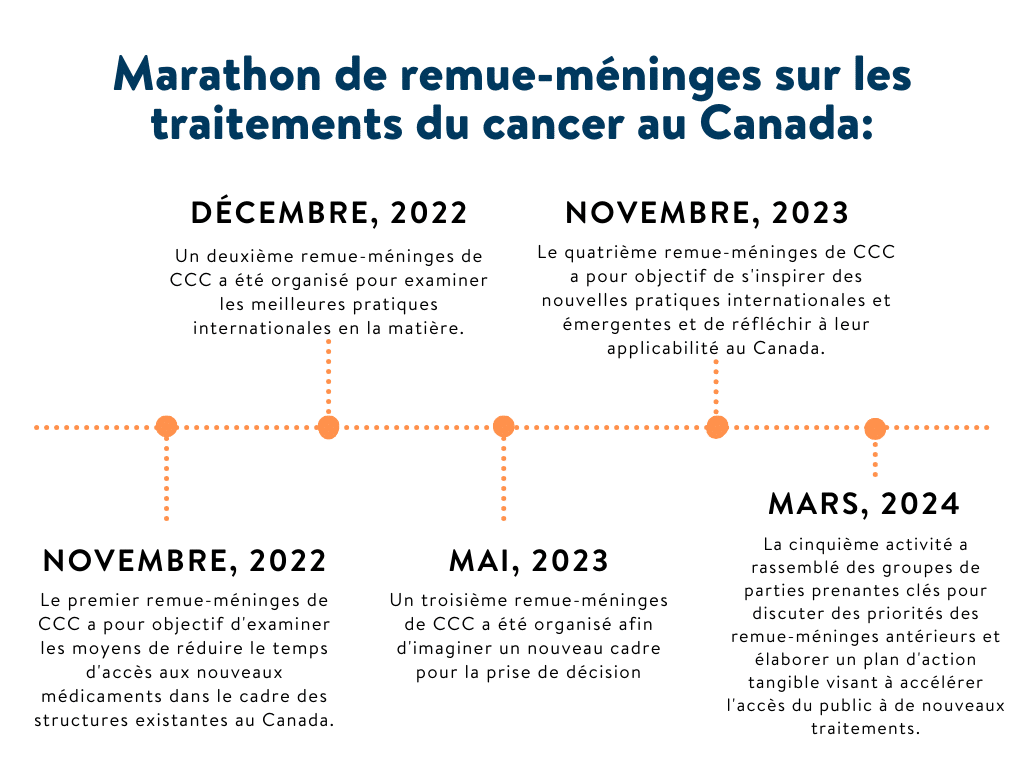
Au cours des deux premières séances de réflexion sur le traitement du cancer au Canada, les participants ont examiné les moyens de raccourcir le délai d’accès aux nouveaux médicaments dans le cadre du processus actuel au Canada, et ont appris d’autres pays qui ont réussi à accélérer le processus d’évaluation des technologies de la santé.
Le troisième Hackathon est allé plus loin en demandant aux participants de concevoir un cadre entièrement nouveau pour la prise de décision concernant l’accès en temps voulu aux nouveaux médicaments au Canada pour les patients.
Lors de notre quatrième événement, les participants ont été invités à s’appuyer sur les idées discutées lors des trois premiers rassemblements et à évaluer comment les pratiques émergentes internationales pourraient être appliquées au Canada afin d’améliorer l’accès aux nouveaux médicaments.
La cinquième activité a rassemblé des groupes de parties prenantes clés pour discuter des priorités mis de l’avant lors des Marathons de remue-méninges antérieurs et a permis d’élaborer un plan d’action tangible visant à accélérer l’accès du public à de nouveaux traitements.
Les activités principales des Marathons de Remue-Méninges de CCC
Figure 2. Calendrier des activités des Marathons de remue-méninges (Hackathon) sur les traitements contre le cancer au Canada
Pour en savoir plus sur les Marathon de remue-méninges (Hackathons), consultez les rapports sur les résultats ci-dessous (disponible en anglais) :
Références :
- Health technology assessment – Global (who.int)
- À propos de L’ACMTS | ACMTS
- Health Technology Assessment Process for Oncology Drugs: Impact of CADTH Changes on Public Payer Reimbursement Recommendations – PMC (nih.gov)
- Accès aux médicaments | Médicaments novateurs Canada
- Statistiques canadiennes sur les cancer – Société canadienne du cancer
- Potential Life‐Years Lost: The Impact of the Cancer Drug Regulatory and Funding Process in Canada – PMC (nih.gov)






































